市场回顾与展望:
沪指短线围绕2900点窄幅波动,医药板块本周表现平平。
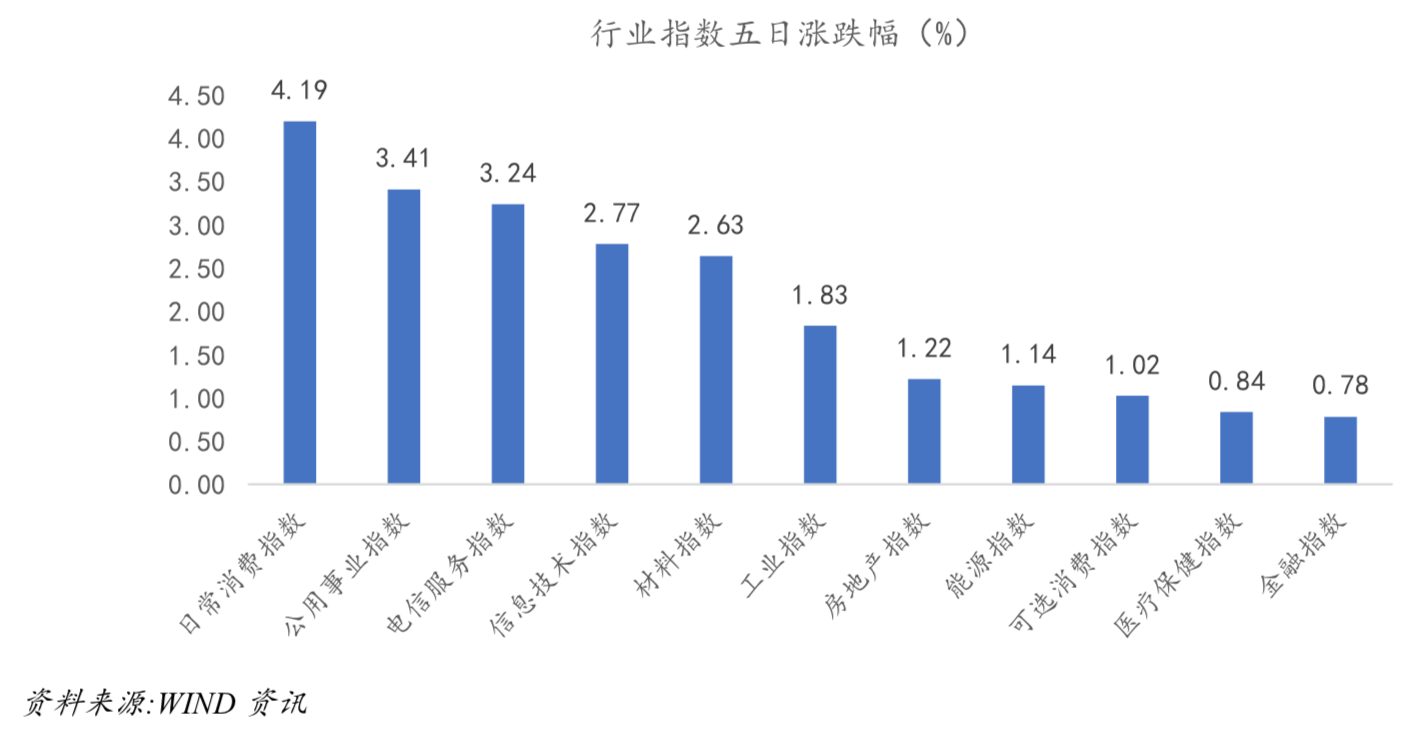
从WIND数据来看,A股市场按GICS一级行业分类,行业指数均录得涨幅,医疗保健指数5日涨幅为0.84%。
截止到目前,制药、生物科技与生命科学板块,医疗保健设备与服务板块的收盘市盈率分别为37.89、30.06倍,较板块过去三年的估值中枢溢价分别为0.02%以及-18.5%。
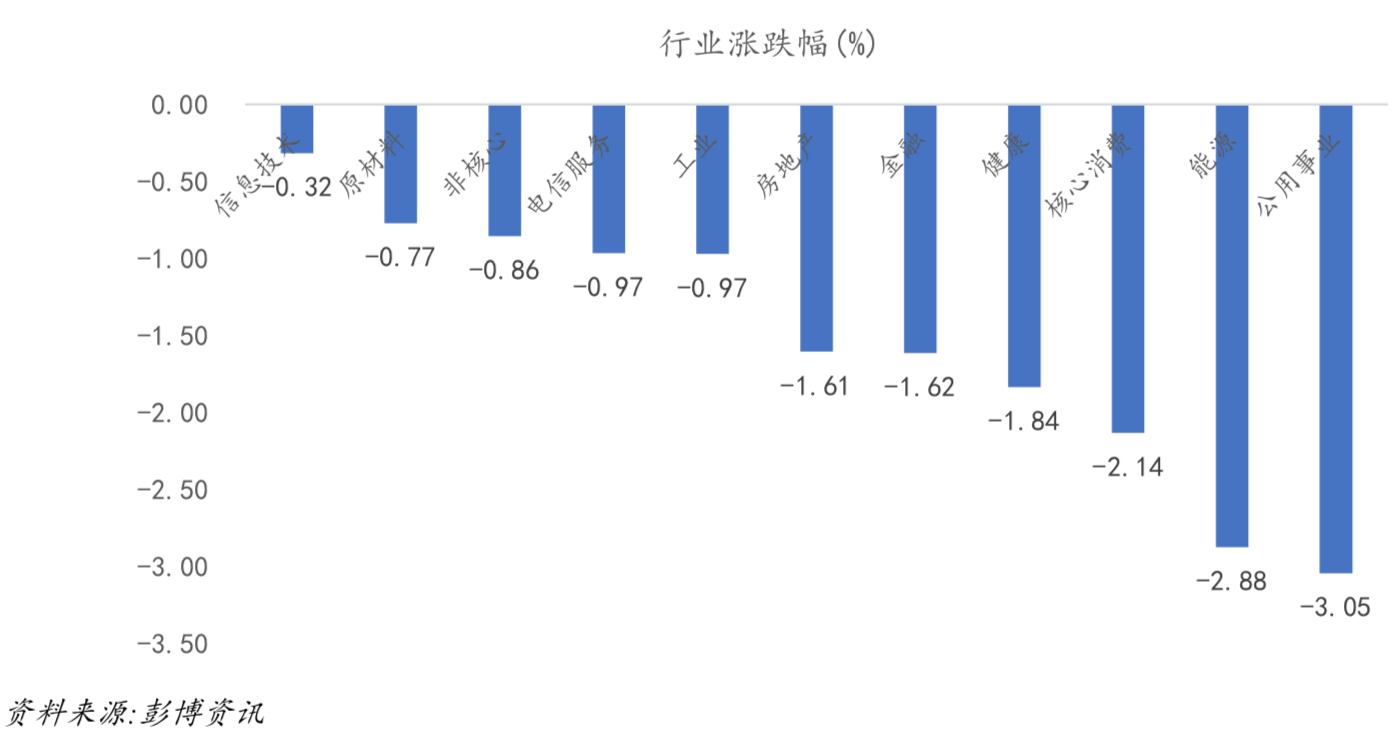
美股方面,根据标普500行业指数表现,行业指数均录得跌幅,排名前五的行业分别为信息技术(-0.32%)、原材料(-0.77%)、非核心(-0.86%)、电信服务(-0.97%)、工业(-0.97%)。
行业观点:
近日,港交所在生物科技周数据显示,截至4月30日,共有11家生物技术和医疗保健公司在港交所提交上市申请,其中9家公司位于中国,这些企业依次有复宏汉霖、盟科生物、迈博医药、亚盛医药、东曜药业、豪森药业、和黄中国医药、康蒂尼药业。包括科创板的推进,生物科技生态圈逐步形成,创新仍将站立政策风口。建议在估值合理下,适当关注研发管线丰富、资金利用效率较高的标的。
一、市场表现回顾
沪指短线围绕2900点窄幅波动,医药板块本周表现平平。近日,港交所在生物科技周数据显示,截至4月30日,共有11家生物技术和医疗保健公司在港交所提交上市申请,其中9家公司位于中国,这些企业依次有复宏汉霖、盟科生物、迈博医药、亚盛医药、东曜药业、豪森药业、和黄中国医药、康蒂尼药业。包括科创板的推进,生物科技生态圈逐步形成,创新仍将站立政策风口。建议在估值合理下,适当关注研发管线丰富、资金利用效率较高的标的。
从WIND数据来看,A股市场按GICS一级行业分类,行业指数均录得涨幅,医疗保健指数5日涨幅为0.84%。
截止到目前,制药、生物科技与生命科学板块,医疗保健设备与服务板块的收盘市盈率分别为37.89、30.06倍,较板块过去三年的估值中枢溢价分别为0.022%以及-18.5%。
美股方面,根据标普500行业指数表现,行业指数均录得跌幅,排名前五的行业分别为信息技术(-0.32%)、原材料(-0.77%)、非核心(-0.86%)、电信服务(-0.97%)、工业(-0.97%)。
二、模拟组合表现
同方模拟医药组合表现vs.医药(中信一级指数)
三、行业动态
1、中国医药产业动态
◆5月26日,泰卫医药信息咨询(上海)有限公司与优锐医药科技联合宣布在中国推出存达®(注射用盐酸苯达莫司汀)产品。存达®适用于在利妥昔单抗或含利妥昔单抗方案治疗过程中或者治疗后病情进展的惰性B细胞非霍奇金淋巴瘤(NHL)。Teva在中国成功实施临床试验并于2016年5月在中国存达®3期研究中获得阳性结果,存达®于2018年12月17日获得中国国家药品监督管理局(NMPA)的上市批准。(资料来源:美通社)
◆5月28日,Viela Bio/豪森药业宣布签订CD19单抗inebilizumab在中国开发用于治疗视神经脊髓炎频谱障碍(NMOSD)和其他自身免疫疾病、血液恶性肿瘤的合作协议。NMOSD是一种罕见自身免疫疾病,患者体内过度活跃的免疫细胞和自身抗体会攻击视神经和脊髓,导致患者会出现失明、截瘫、感觉丧失、膀胱失调、以及外周疼痛等症状。目前尚无任何针对这种罕见病的疗法获批。inebilizumab可以结合B细胞表面的CD19抗原,耗竭CD19+B细胞。在今年4月刚被FDA授予治疗NMOSD的突破性疗法资格。(资料来源:医药魔方网)
◆5月29日,FDA授予ZW25快速通道资格,以加速ZW25联合化疗用于HER2高表达的胃癌患者。ZW25是Zymeworks的一项重要资产,快速通道资格将会进一步加速该药物的上市进程。
ZW25定位于best-in-class,目前两个适应症处于临床开发阶段,其中HER2高表达的胃癌处于2期临床。2018年11月27日,百济神州获得ZW25在亚洲(日本除外)、澳大利亚和新西兰的独家开发和商业化权益。(资料来源:新浪医药网)
◆5月29日,CDE发布了《真实世界证据支持药物研发的基本考虑(征求意见稿)》指出,考虑到药物临床研发过程中,存在临床试验不可行或难以实施等情形,利用真实世界证据用以评价药物的有效性和安全性成为可能的一种策略和路径。(资料来源:医药地理网)
◆5月29日,国家药监局药品审评中心(CDE)发布通知,正式将Biopten Granules 等26个无异议的品种作为第二批临床急需境外新药品种名单正式对外发布。本次公布的名单比三月份公布的名单相比少了5个,其中退出的包括诺和诺德地特胰岛素注射液和第一三共株式社会的Inavir、日本盐野义制药和罗氏联合申报的Xofluza、赛诺菲的Praluent Alirocumab、Santen OY公司Verkazia等。新增的品种有新增诺和诺德NORDITROPIN(somatropin)injection,该产品主要用于治疗罕见病。目前该药已经在国内获批进口,商品名为“诺泽”。(资料来源:新浪医药网)
◆近日,江苏省无锡市卫健委印发《2019年全市卫生健康工作要点》,明确表态将与国家药品4+7带量采购价格联动,做好降价药品进医院工作。如果一切顺利,江苏全省就将在今年末或明天初,跟进4+7。(资料来源:赛柏蓝公众号)
2、海外医药产业动态
◆5月27日,诺华PI3K抑制剂获FDA批准用于乳腺癌治疗。FDA批准诺华公司开发的alpelisib与氟维司群联用,二线治疗携带PIK3CA基因突变的HR+/HER2-晚期或转移性乳腺癌患者。这是FDA批准的第一款用于治疗乳腺癌的PI3K抑制剂。此次批准是基于名为SOLAR-1的3期临床试验。试验结果表明,在携带PIK3CA基因突变的乳腺癌患者中,与对照组相比,alpelisib与氟维司群联用,能够显著提高患者的中位无进展生存期(11个月比5.7个月)(资料来源:FDA官网)
◆5月28日,血友病基因疗法3期临床达到主要终点。A型血友病是一种由于遗传原因导致凝血因子VIII缺失的血液疾病。对严重A型血友病患者的标准治疗方法是预防性凝血因子VIII静脉注射。BioMarin公司开发的valoctogogene roxaparvovec是一种使用AAV5载体递送表达凝血因子VIII的转基因的基因疗法。它的优势在于患者可能只需要接受一次治疗,就可以获得表达凝血因子VIII的基因,从而不再需要长期接受预防性凝血因子注射。16名接受治疗的患者平均年出血率为1.5,与接受标准预防疗法的患者相比,降低了85%。同时,患者的年度凝血因子VIII用量减少84%,在接受治疗后5-26周之间,患者的年度凝血因子VIII用量减少94%。(资料来源:BioMarin官网)
◆5月29日,高纯度鱼油Vascepa获FDA优先审评资格。Amarin公司研发的Vascepa是由高纯度的icosapent ethyl组成,源于天然鱼油成分ω-3脂肪酸。Vascepa是一种处方药,被FDA认定为新化学实体,并非普通鱼油类的膳食补充剂。此次sNDA申请是基于名为REDUCE-IT的大型3期临床试验。试验结果显示,Vascepa可将首次发生主要不良心血管事件(MACE)的风险相对降低25%。此次sNDA申请被授予优先审评资格,预计19年9月前会收到FDA的回复。(资料来源:Amarin官网)
◆5月30日,来那度胺联用利妥昔治疗FL/MZL获FDA批准。这是FDA批准的第一款治疗滤泡性淋巴瘤(FL)或边缘区淋巴瘤(MZL)等惰性非霍奇金淋巴瘤(NHL)的非化疗组合疗法。此次批准是基于名为AUGMENT的3期临床试验,共计有295名FL和65名MZL患者加入了临床试验。试验结果表明,来那度胺与利妥昔单抗构成的组合疗法(R2),与利妥昔单抗和安慰剂构成的对照组相比,显著提高患者的无进展生存期(PFS)。R2疗法的中位PFS为39.4个月,对照组为14.1个月,提升一倍以上。(资料来源:FiercePharma)
◆5月31日,诺华哮喘疗法3期临床达到主要终点。QMF149是一款每日一次的固定剂量的吸入性复方药物,由长效β2受体激动剂茚达特罗和皮质类固醇糠酸莫米松两种有效成分构成。在名为QUARTZ的3期临床试验中,哮喘控制不充分的患者分别接受低剂量的QMF149或糠酸莫米松的治疗。试验结果显示,在12周后,与对照组相比,QMF149低剂量组,不仅达到了显著改善患者的肺功能这一主要终点,将1秒用力呼气量(FEV1)平均提高了182毫升,还将患者晚间呼气峰值流量(evening PEF)提高26.1升/分钟,而这进一步显示了QMF149对肺功能临床意义上的改善。此外,在第12周时,与对照组相比,QMF149低剂量组在哮喘问卷评分(ACQ-7)方面显示了对哮喘控制的统计学显著改善,并且得到缓解的比例更高(74.7%对比64.9%),达到了试验的次要终点。(资料来源:FierceBiotech)
四、上市公司公告
【华东医药】5月26日公告,拟以不超过10.6亿元受让佐力药业1.13亿股股份,占佐力药业总股份比例为18.60%,该事项的履行将可能导致佐力药业控制权发生变更。佐力药业主要业务为药用真菌系列产品、中药饮片及中药配方颗粒的研发、生产与销售。主要产品包括乌灵胶囊、灵莲花颗粒、灵泽片、百令片、中药饮品片和中药配方颗粒。2018年佐力药业实现营业收入7.3亿元,比上年同期减少8.02%;实现归母净利润2075.18万元,比上年同期减少54.03%。(资料来源:WIND资讯)
【中国生物制药】 5月28日公告,附属公司正大天晴药业集团开发的预防恶心和呕吐药“盐酸帕洛诺司琼注射液”获国家药监局批准增加1.5ml:0.075mg规格及新增“预防术后恶心和呕吐”适应症。据米内网数据,2017年中国公立医疗机构终端帕洛诺司琼销售额为16.88亿元。本次获批后,正大天晴盐酸帕洛诺司琼注射液(商品名止若)“预防化疗药后呕吐”适应症扩展至儿童人群,同时新增“预防术后恶心和呕吐”适应症;该药物原有规格为5ml:0.25mg,现新增1.5ml:0.075mg规格。正大天晴于2008年获得盐酸帕洛诺司琼注射液的药品注册批件。(资料来源:WIND资讯)
【四环医药】5月29日公告,该公司自主研发1类创新药第三代EGFR 抑制剂XZP-5809已获得国家药监局颁发的药物临床试验批件。四环医药此次获批的XZP-5809是一种新型第三代表皮生长因子受体酪氨酸激酶抑制剂,候选物的临床适应症拟定为治疗具有EGFR敏感突变(19位外显子缺失和L858R突变)和获得性耐药突变(T 790M突变)的局部晚期或转移性肺癌等实体瘤。(资料来源:WIND资讯)
【爱尔眼科】5月29日公告,其拟收购重庆儿童眼科85%的股权。根据重庆儿童眼科现有的业务、资产、人才和技术的基础,经交易各方协商一致,重庆儿童眼科85%股权交易价格为4250万元。收购完成后,爱尔眼科将持有重庆儿童眼科85%的股权。重庆儿童眼科,成立于2018年6月,专门为0-18岁儿童提供眼科医疗服务。2019年1月25日,重庆儿童眼科获得医疗机构职业许可证,目前仍处于试营业阶段。(资料来源:WIND资讯)
【绿叶制药】5月29日公告,美国食品药品监督管理局(“FDA”)已经完成立卷审查并决定受理集团研发的Rykindo(LY03004)(为每两周注射一次的缓释微球肌肉注射制剂,乃根据联邦食品、药品和化妆品法案的第505(b)(2)条及联邦规则汇编第21章§314.50用于治疗精神分裂症及双相情感障碍一型)的新药申请。(资料来源:WIND资讯)
【海正药业】 5月30日公告,将以公开挂牌方式转让参股公司浙江导明医药科技有限公司20.24%的股权,该股权对应的评估价值为1.38亿元。本次股权转让是导明医药为实现境外上市而实施的股权重组整体方案中的一部分。除对外转让20.24%的股权外,海正药业还将同意在境外设立全资子公司,将所持有的导明医药的19.8%股权转由境外全资子公司间接持有。(资料来源:WIND资讯)
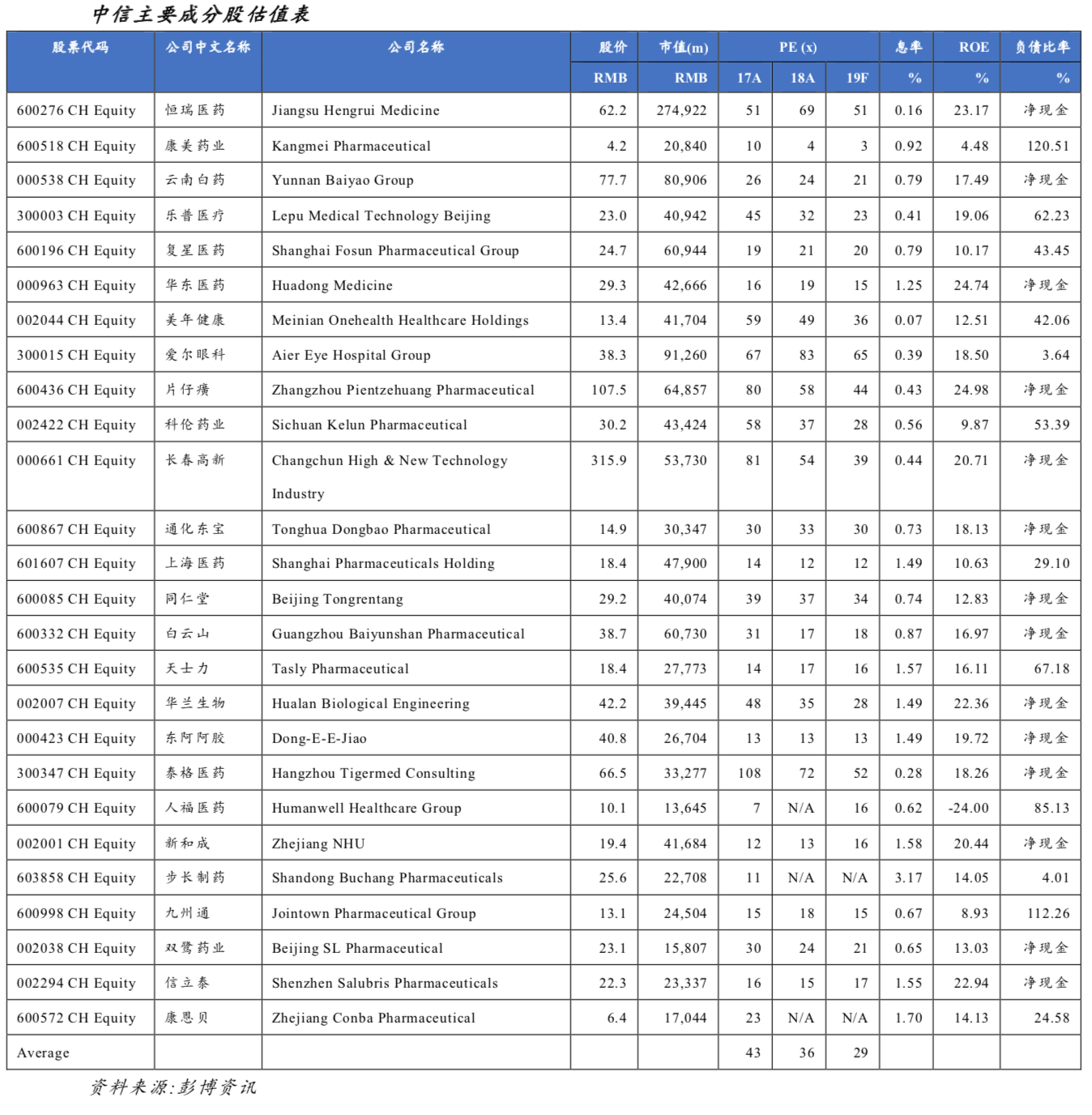
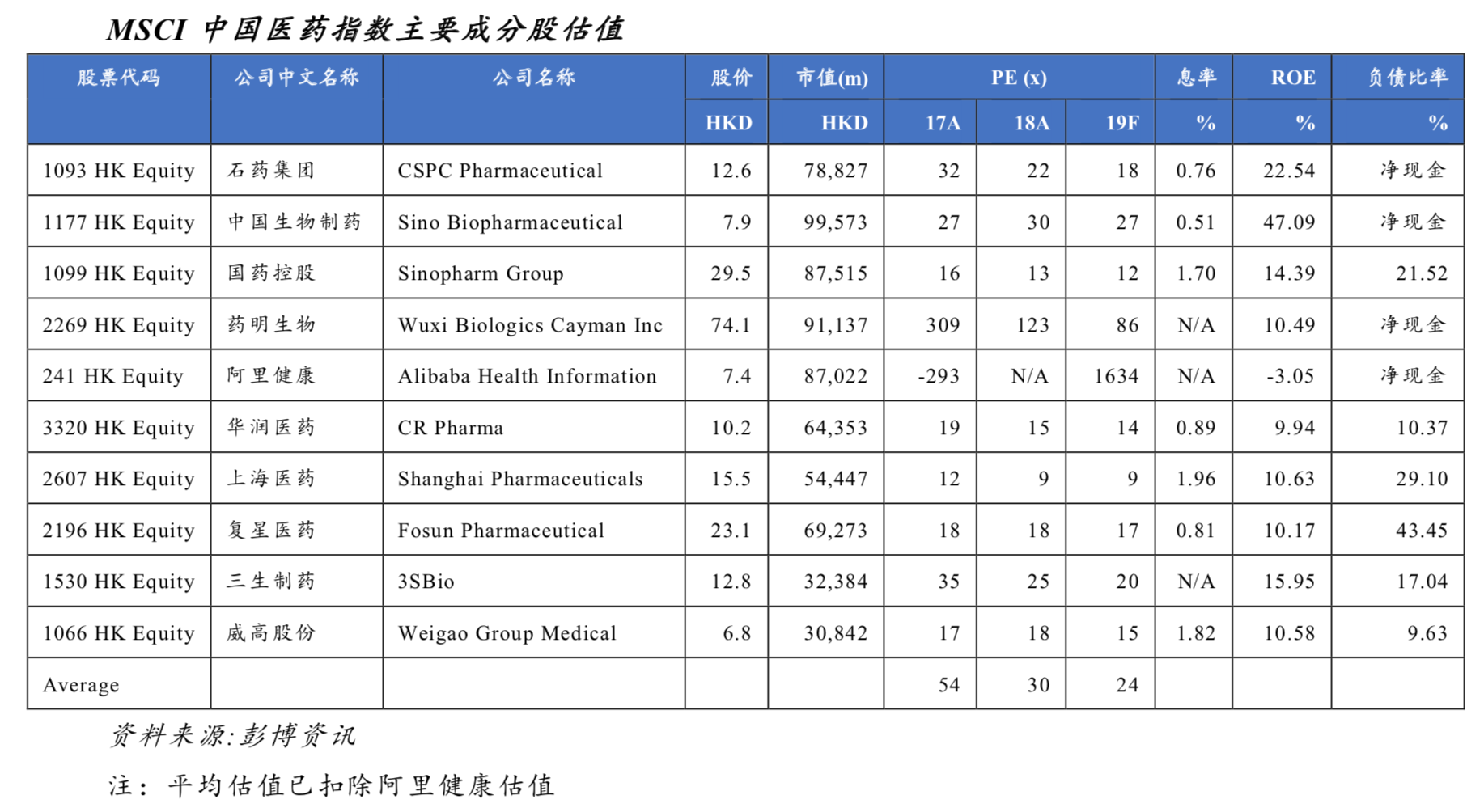
五.MSCI中国医药和中信医药主要成分股估值
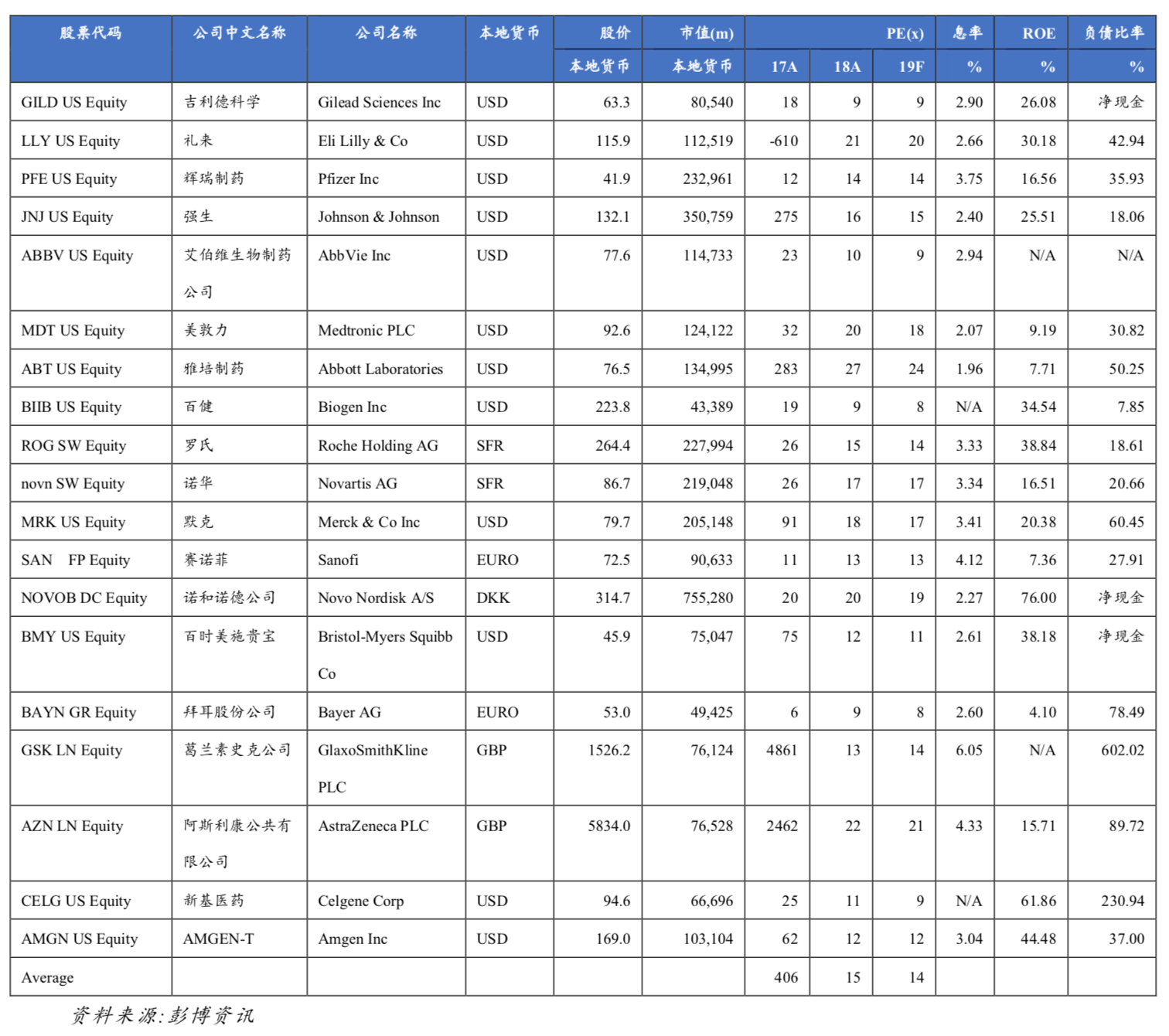
六、国际大药厂估值图
七、风险提示
1、药企研发风险:研发时间增加、投入加大、研发数据结果低于预期的风险
2、新药上市后风险:安全性风险、市场竞争、销售低于预期的风险
3、政策不可预知的风险
4、招标降价的风险
免责声明:本文内容既不代表同方研究的推荐意见,也不构成所涉及的个别股票的买卖或交易要约。在作出任何投资决定前,投资者应根据自身情况考虑投资产品相关的风险因素,并于需要时咨询专业投资顾问意见。



精彩评论